Die Afrikanische Trypanosomiasis ist eine durch Unterarten von Trypanosoma brucei ausgelöste Tropenerkrankung, die auch als (Afrikanische) Schlafkrankheit bezeichnet wird. Sie kommt in den tropischen Gebieten Afrikas vor und wird von der Tsetsefliege übertragen, verursacht durch die in ihr lebenden Protozoen. Die Erkrankung verläuft in drei Stadien und wird meist chronisch: Einige Wochen nach der Infektion kommt es zu Fieber, Schüttelfrost, Ödemen, Lymphknotenschwellung sowie Hautausschlag und Juckreiz. Im zweiten Stadium nach einigen Monaten stehen Symptome des Nervensystems im Vordergrund: Verwirrtheit, Koordinations- und Schlafstörungen sowie Krampfanfälle. Im Endstadium fällt der Patient in einen schläfrigen Dämmerzustand (Schlafsucht), der der Krankheit ihren Namen gegeben hat. Der Nachweis der Erreger erfolgt mikroskopisch im Blut oder dem Liquor cerebrospinalis sowie mit immunologischen Methoden. Zur Behandlung stehen mehrere Wirkstoffe zur Verfügung.
Die Schlafkrankheit wird durch humanpathogene Einzeller (Protozoen) aus der Gruppe der Trypanosomen hervorgerufen. Man unterscheidet zwei Erregertypen:
Trypanosoma brucei gambiense (Erreger der Westafrikanischen Schlafkrankheit)
Trypanosoma brucei rhodesiense (Erreger der Ostafrikanischen Schlafkrankheit)
Afrikanische Trypanosomen wurden erstmals 1895 vom Arzt David Bruce im Blut von an Nagana erkrankten Rindern beobachtet und als Auslöser der Erkrankung identifiziert. Auch die Übertragung durch Tsetsefliegen konnte Bruce zeigen. Der Erreger wurde zu Ehren von Bruce Trypanosoma brucei (Synonym: Trypanosoma hominis) genannt. Wenige Jahre später wurden Trypanosomen in an der Westafrikanischen Schlafkrankheit erkrankten Menschen identifiziert; der 1902 von Aldo Castellani als Ursache der Schlafkrankheit erkannte Erreger wurde nach dem westafrikanischen Fluss Gambia Trypanosoma gambiense genannt; dort wurde der Parasit zum ersten Mal identifiziert. Auch bei an der Ostafrikanischen Schlafkrankheit erkrankten Patienten wurden (zuerst von Robert Koch) Trypanosomen gefunden, die nach der britischen Kolonie Nordrhodesien, dem Ort der ersten Identifizierung, Trypanosoma rhodesiense genannt wurden. Die drei ursprünglich identifizierten Arten wurden 1972 zu einer Art unter dem Namen Trypanosoma brucei zusammengefasst, die wiederum in drei Unterarten, Trypanosoma brucei brucei, Trypanosoma brucei gambiense und Trypanosoma brucei rhodesiense aufgeteilt wurde.
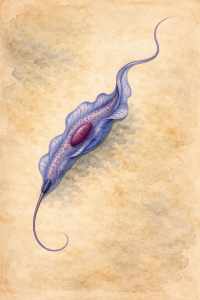
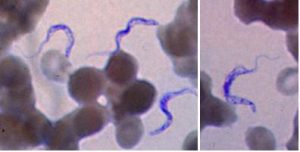
Der Einzeller hat eine einzelne Geißel, die an der Zelloberfläche unter einer undulierenden Membran zum Vorderende der Zelle verläuft und dort bei den meisten Formen des Parasiten zu einer freischwingenden Geißel wird. Ferner haben die Zellen einen kleinen Kinetoplasten, einer Ansammlung von DNA innerhalb eines großen Mitochondriums. Der Parasit kommt in mehreren pleomorphen Zellformen vor:
Die trypomastigote Form, bei der die Basis der Geißel posterior zum Zellkern liegt, kommt im Blut von Säugetieren entweder als schlanke, bis zu 40 µm lange Form (slender) mit langer, freier Geißel und subterminalem Kinetoplast oder als kurze, gedrungene, bis zu 25 µm lange Form (stumpy) ohne freies Geißelende sowie einem Kinetoplasten nahe dem posterioren Ende vor; dazwischen gibt es noch intermediäre Formen. Ferner unterscheidet man eine prozyklische und eine metazyklische Form; beide kommen in Tsetse-Fliegen vor. Die metazyklische Form hat keine freie Geißel.
Die epimastigote Form, bei der die Geißelbasis und der Kinetoplast anterior zum Zellkern liegt, ist der trypomastigoten ansonsten ähnlich und kommt ebenfalls nur in Fliegen vor.
Mikroskopisch sind die drei Unterarten nicht zu unterscheiden. Auch die Arten Trypanosoma evansi, Erreger der Surra, und Trypanosoma equiperdum, Erreger der Beschälseuche, sind mikroskopisch nicht von Trypanosoma brucei unterscheidbar.
Alle drei Unterarten von Trypanosoma brucei kommen praktisch ausschließlich in Afrika südlich der Sahara im Verbreitungsgebiet der Tsetsefliege, im sogenannten Tsetsegürtel, vor. Die Verbreitungsgebiete von Trypanosoma brucei gambiense und Trypanosoma brucei rhodesiense sind durch den ostafrikanischen Grabenbruch getrennt; lediglich in Uganda werden beide Unterarten beobachtet, allerdings in getrennten Verbreitungsgebieten. Trypanosoma brucei brucei ist im gesamten Tsetsegebiet anzutreffen.
Für Trypanosoma brucei gambiense ist der Mensch das Hauptreservoir. Der Erreger wurde zwar auch aus Schweinen und Schafen, in Einzelfällen auch aus Affen isoliert, die epidemiologische Bedeutung als Reservoir ist aber umstritten. Affen können experimentell infiziert werden, ohne ernsthaft zu erkranken. Übertragen werden diese Parasiten von Fliegen der Glossina palpalis-Gruppe, die vorwiegend in der Nähe von Flussläufen leben. Der Grund für die Anfälligkeit des Menschen für die Infektion mit diesem Erreger liegt in der Resistenz des Erregers gegen zwei menschliche Proteine, die trypanolytischen Faktoren (TLF-1 und TLF-2).
Für Trypanosoma brucei rhodesiense ist das Rind das Hauptreservoir; in Epidemiegebieten können bis zu 20 Prozent der Rinder akut oder auch chronisch mit humanpathogenen Parasiten infiziert sein. Neben dem Rind sind Haustiere wie das Schwein oder die Ziege weitere Reservoirs. Auch aus verschiedenen Wildtiere, beispielsweise dem Buschbock und anderen Antilopen, wurden oft Parasiten isoliert. Epidemiologisch spielen Wildtiere aufgrund der zurückgehenden Verbreitungsräume der Tiere keine dominierende Rolle mehr, es können aber ausgehend von Wildtierreservoirs Haustiere und in der Folge Menschen infiziert werden. Eine experimentelle Infektion ist bei Affen möglich und in den meisten Fällen tödlich. Die Übertragung erfolgt durch Fliegen der Glossina morsitans-Gruppe, die vorwiegend in der Savanne leben, sowie durch Bremsen der Gattung Chrysops.
Trypanosoma brucei brucei kann viele Haussäugetiere, Kamele, sowie zahlreiche Wildtiere, darunter verschiedene Antilopen und einige Karnivoren, aber nicht den Menschen infizieren. Der Verlauf der Infektion ist sehr unterschiedlich; so zeigen manche westafrikanischen Hausrind-Rassen kaum Krankheitszeichen, während ostafrikanische Zebu-Rinder besonders empfindlich sind. Infektionen bei Pferden, Kamelen, Hunden und Katzen verlaufen meist schwer und sind oft tödlich. Für die Resistenz des Menschen gegenüber Trypanosoma brucei brucei und mancher anderer Trypanosomen ist das Apolipoprotein L-I (APOL1) verantwortlich, ein Protein, das zuerst beim Menschen und bei Gorillas gefunden wurde. Wenn Trypanosomen APOL1 durch Endozytose aufnehmen, bildet APOL1 in der Membran der Lysosomen Poren, die zu einer Lyse der Parasitenzellen führen. Erkauft wird dieser Selektionsvorteil aber durch ein erhöhtes Risiko, an bestimmten Nierenkrankheiten (Nephrosklerose, Fokal segmentale Glomerulosklerose) zu erkranken, deren Häufigkeit bei Menschen schwarzafrikanischer Abstammung entsprechend erhöht ist. Die Serumresistenz des Menschen durch APOL1 wird von Trypanosoma brucei rhodesiense mittels des Serum Resistance Associated (SRA)-Faktors überwunden, indem das SRA-Protein an das Apolipoprotein bindet und dessen trypanolytische Wirkung neutralisiert. Trypanosoma brucei gambiense hat kein SRA; der Mechanismus der Serumresistenz bei dieser Unterart ist unbekannt.
Trypanosomen können prinzipiell auch mechanisch übertragen werden, beispielsweise durch medizinisches Besteck. Eine Übertragung von der Mutter auf den Embryo kommt vor, spielt jedoch epidemiologisch keine Rolle; eine Übertragung durch Transfusionen erscheint möglich, ist aber nicht dokumentiert. Eine rein mechanische Übertragung durch Wadenstecher ist experimentell nachgewiesen, die epidemiologische Bedeutung aber unklar. Es gibt aber Hinweise auf Fälle der Nagana mit Trypanosome brucei. außerhalb des Tsetse-Verbreitungsgebietes.
Trypanosoma brucei vermehrt sich ausschließlich extrazellulär. Nach dem Stich einer infizierten Tsetsefliege gelangen mit dem Speichel metazyklische trypomastigote Zellen ins Gewebe des Säugetierwirtes, wo sie sich im Zellzwischenraum zu schlanken Trypomastigoten umwandeln und durch Längsteilung vermehren. Von dort gelangen die Zellen ins lymphatische System und in die Blutbahn, wo sie sich weiter vermehren. Im weiteren Verlauf der Infektion wandeln sich die schlanken Trypomastigote teilweise in kurze, gedrungene Trypomastigote um; diese vermehren sich nicht mehr, sind aber infektiös für die Fliegen. Ausgehend von den Parasiten im Blutstrom kann auch das zentrale Nervensystem befallen werden, was dann zu den Symptomen der Afrikanischen Schlafkrankheit führt.
Wenn eine Tsetsefliege ein infiziertes Säugetier sticht, kann sie auf diesem Wege mit dem Blut Parasitenzellen aufnehmen. Durch solch eine Blutmahlzeit aufgenommene gedrungene Trypomastigote wandeln sich in der Fliege im Mitteldarm zu prozyklischen Trypomastigoten um. Dabei ändert sich massiv die Zelloberfläche des Parasiten: die Hülle aus variablen Oberflächenglykoproteinen wird durch einen Oberflächenmantel aus Prozyklin-Protein ausgetauscht; gleichzeitig wird der Energiestoffwechsel von einer in einem speziellen Organell, dem Glycosom ablaufenden glykolytischen auf eine oxidative ATP-Generierung im Mitochondrium umgestellt.
Die prozyklischen Trypomastigoten vermehren sich im Darm der Fliege, wandeln sich zu Epimastigoten um und wandern in die Speicheldrüse, wo sie sich weiter vermehren. Epimastigote sind die einzige Form des Parasiten, die durch Rekombination genetische Informationen austauschen können; Mehrfachinfektionen mit verschiedenen Trypanosomen werden in Tsetsefliegen häufig beobachtet, sodass ein regelmäßiger genetischer Austausch möglich erscheint. Aus den Epimastigoten entstehen schließlich in der Speicheldrüse neue metazyklische trypomastigote Zellen, die erneut eine Hülle aus variablen Oberflächenglykoproteinen tragen. Diese Zellen können über den Speichel der Fliege nach einem Stich einen neuen Säugetierwirt infizieren. Der Vermehrungszyklus in der Fliege dauert 20 bis 40 Tage; die Fliegen bleiben für ihre gesamte Lebensdauer infektiös.
Nicht alle Tsetsefliegen sind Trypanosomen-Überträger, sodass nicht jeder Stich zwangsläufig zu einer Infektion führt. Das Infektionsrisiko bei einem Stich ist regional sehr unterschiedlich und liegt durchschnittlich in der Größenordnung von 1 %, denn auch die Durchseuchungsrate der Tsetsefliege variiert stark. Das Risiko steigt also mit der Zahl der Stiche. Die Infektion trifft überwiegend die einheimische Bevölkerung, seltener Touristen.
Welche Tierarten bei der Übertragung auf den Menschen die bedeutendste Rolle spielen, ist nicht abschließend geklärt, da ein kompliziertes Geflecht von anderen epidemiologischen Parametern beachtet werden muss (z. B. 31 Tsetse-Arten mit Vorlieben für bestimmte Wirtstiere, sowie Regenzeiten, soziale Faktoren, unterschiedliche Erregerstämme etc.). Das Infektionsrisiko ist deswegen lokal und regional sehr unterschiedlich.